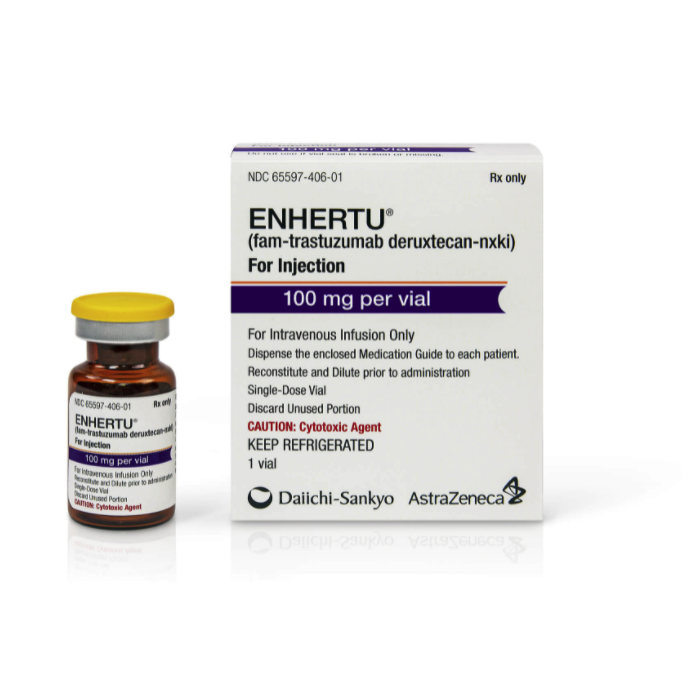
Enhertu 治疗肺癌:在哪里获批,如何获得?
最后更新2024 年 1 月 16 日
你可以合法地获得新药,即使它们在你的国家没有得到批准。
了解更多 "Enhertu (fam-trastuzumab deruxtecan-nxki) 自 2019 年首次获得美国食品及药物管理局批准1 以来,一直是值得关注的癌症治疗方法之一。
由于Enhertu 对卵巢癌和结直肠癌的安全性和有效性仍在研究中,该药已被批准用于多个适应症。包括 HER2 阳性乳腺癌、HER2 阳性胃癌和 HER2 低度乳腺癌。美国 FDA 还批准Enhertu 用于治疗 HER2 突变的非小细胞肺癌。欧洲的 CHMP 最近也给出了积极的意见,同意在欧盟2.
如果您是英国或美国和欧盟以外其他国家的肺癌患者,您可能想知道Enhertu 何时也能为您所用。
以下是有关Enhertu 治疗肺癌的所有信息,以及英国和世界其他地区的患者可以期待的治疗。
Enhertu 治疗肺癌的适应症是什么?
作为一种靶向疗法,Enhertu 只用于治疗 HER2 基因突变的癌症。因此,这种疗法适用于大约 2% 的 NSCLC 患者3。
Enhertu Enhertu 的目标患者是既往接受过全身治疗、癌症已扩散至身体其他部位或无法通过手术切除的晚期 NSCLC 患者。
Enhertu 治疗肺癌的成功率有多高?
目前正在进行的 DESTINY-Lung02 II 期试验正在研究Enhertu 治疗 HER2 突变 NSCLC 的安全性和有效性。该试验对两种剂量的Enhertu (5.4 毫克/千克和 6.4 毫克/千克)进行了比较。
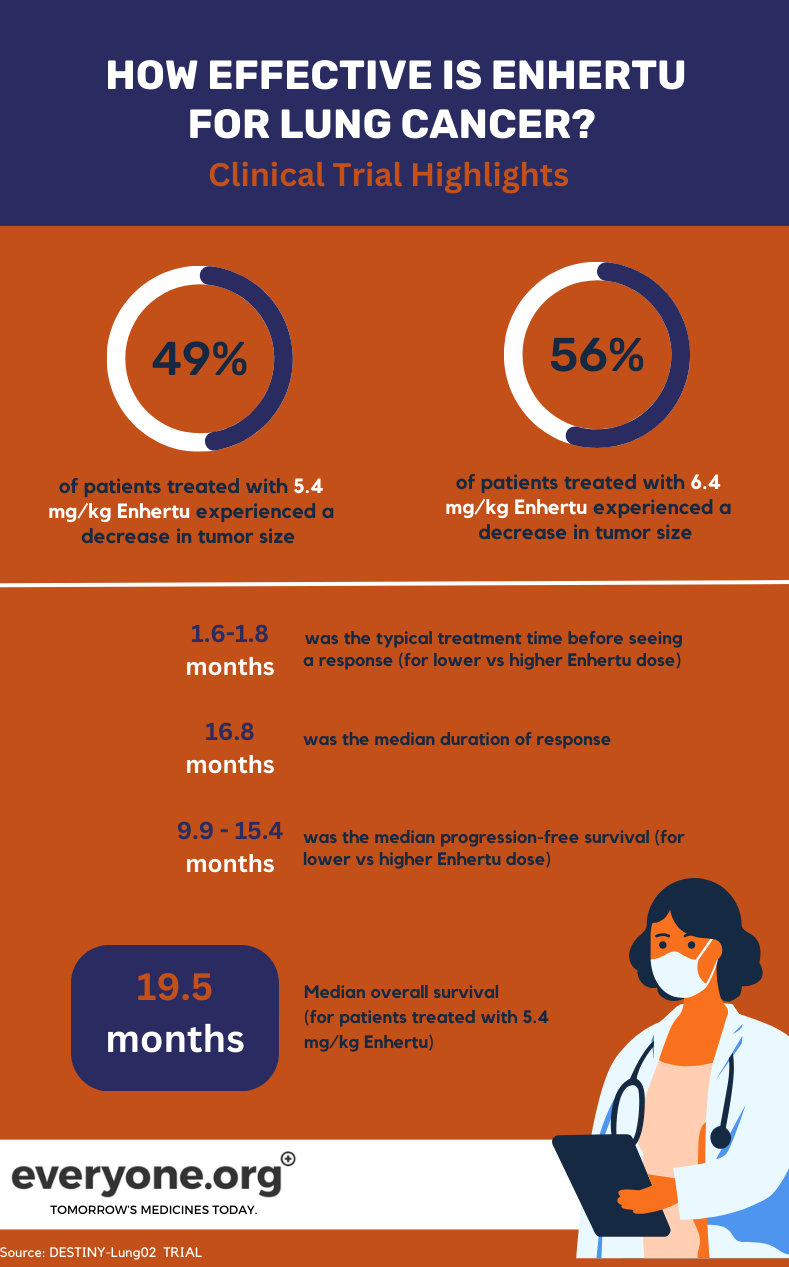
对于肺癌患者来说,DESTINY-Lung02 试验的主要初步结果是
- 在接受低剂量Enhertu 治疗的患者中,49%的肿瘤缩小了,而在接受高剂量治疗的患者中,56%的肿瘤缩小了。
- 低剂量组和高剂量组分别有 1%和 4%的患者肿瘤完全消失。
- Enhertu 低剂量组患者的中位反应持续时间为 16.8 个月。另一组患者的反应持续时间无法估计。
- 低剂量组和高剂量组观察到初始治疗反应所需的中位时间分别为 1.8 个月和 1.6 个月。
- 5.4 毫克/千克的中位无进展生存期为 9.9 个月,6.4 毫克/千克的中位无进展生存期为 15.4个月。
Enhertu 患者的中位生存期有多长?
在临床试验中,接受低剂量Enhertu 的患者的中位总生存期(OS)为 19.5 个月。据报告,高剂量组4 的 OS 无法估计。
Enhertu 对肺部有什么副作用?
Enhertu 患者中出现过一些严重的、危及生命或致命的间质性肺病(ILD)病例。中度肾功能损害患者的风险可能更高6.
在 DESTINY-Lung02 试验中,低剂量组有 12.9% 的患者报告了 ILD,高剂量组有 28% 的患者报告了 ILD。其中大多数病例并不严重。两组患者中均有 2% 的患者出现 3 级或更严重的 ILD。
Enhertu肺癌的安全性与其在其他适应症中的表现相似。由于不良反应发生率较低(38.6% 对 58%),5.4 mg/kg 剂量被认为是治疗 NSCLC 患者的最佳剂量。

Enhertu 在哪里被批准用于治疗肺癌?
目前,Enhertu 已在美国、以色列和日本获得批准,用于治疗肿瘤有激活 HER2(ERBB2)突变的不可切除或转移性 NSCLC 成年患者4。根据CHMP的积极意见2,EMA也即将正式批准该药。
Enhertu 在英国被批准用于治疗肺癌吗?
截至 2023 年 11 月,还没有。NICE 的审查预计将于 2024 年 7 月中旬开始5。如果审查结果良好,Enhertu 可能会在 2024 年底向英国 HER2 突变 NSCLC 患者提供。遗憾的是,在此之前,Enhertu 还不能在英国用于肺癌治疗。
如果Enhertu 尚未获得批准,我的医生能否为我开具治疗肺癌的处方?
简而言之,答案是肯定的。
Enhertu 已被多个国家批准用于治疗 HER2 突变的 NSCLC。因此,即使该药尚未在您所在的国家获得批准,您的医生也有权根据这一适应症开具处方。
当医生开出治疗某种疾病的处方时,如果该药尚未获得批准(尚未获得批准),这就是标示外使用。标示外使用处方在某些国家可能难以开具,这取决于当地的法规和供应情况。不过,使用 "指定患者进口条例 "配药总是可行的。
您的医生是否已决定为您开Enhertu 治疗肺癌?我们位于 www.everyone.org 的团队可以帮助您获得这种药物。我们专门从事采购和交付未经批准或患者所在国无法获得的处方药。请联系我们,我们将为您提供帮助。
参考文献:
- Stewart, Judith.Enhertu (fam-trastuzumab deruxtecan-nxki) FDA 批准历史。Drugs.com,2022 年 8 月 15 日。
- Enhertu.欧洲药品管理局,2023 年 11 月 6 日访问。
- HER2 与肺癌。美国肺脏协会,2023 年 11 月 6 日访问。
- Enhertu 在 DESTINY-Lung02 II 期临床试验中,HER2 突变晚期肺癌患者的肿瘤反应强烈而持久。阿斯利康,2023 年 9 月 11 日。
- 项目信息 | 曲妥珠单抗德鲁司坦用于治疗 HER2 突变的、经 1 种或多种疗法后不可切除或转移的非鳞状非小细胞肺癌 [ID3934] | 指南。NICE,2023 年 11 月 6 日访问。
- USPI-DB-04 CDX Update FINAL.Daiichi Sankyo, 2023 年 11 月 6 日访问。