Enhertu 可以治疗结直肠癌吗?最新结果、批准时间表等。
最后更新2024 年 1 月 15 日
你可以合法地获得新药,即使它们在你的国家没有得到批准。
了解更多 "自 2019 年首次获得 FDA 批准以来、 Enhertu在肿瘤学界获得了广泛关注。2023 年,Enhertu ,继续其令人瞩目的发展轨迹,又获得两项 FDA 突破性认定。现在,它总共拥有 7 项1.
Enhertu 的最新突破性成果之一是用于治疗 HER2 阳性转移性结直肠癌2。对于所有结直肠癌患者来说,这是一个重要的里程碑。同时,它也提出了许多问题。
以下是有关Enhertu 大肠癌的所有信息。
Enhertu 的突破性指定是否等同于 FDA 批准?
突破性疗法认定并不自动意味着获得 FDA 批准。不过,它也有一些好处,例如在药品开发过程中可以得到强化指导和高级管理层的参与。这些优势有助于加快药品的后续审批3.
Enhertu 被批准用于治疗哪些类型的癌症?
Enhertu 目前已获得欧洲药品管理局(EMA)批准,用于治疗以下疾病
- 无法通过手术切除的 HER2 阳性转移性乳腺癌;
- HER2 低的转移性乳腺癌,无法通过手术切除;
- HER2 阳性晚期胃癌(胃癌)或胃食管交界癌4.
在美国,Enhertu 还被批准用于治疗以下疾病:
- HER2 突变转移性非小细胞肺癌5.
Enhertu 治疗大肠癌的效果如何?
由于Enhertu 是一种靶向疗法,因此只适用于 HER-2 表达的癌症。在所有结直肠癌中,约有 3%-5% 属于这一类 6。
临床试验结果
2023 年 6 月,DESTINY-CRC01 试验的最终结果公布。这项 2 期试验的重点是评估Enhertu 对表达 HER2 的转移性结直肠癌患者的疗效和安全性。参加试验的患者的肿瘤至少在之前两轮治疗后出现了进展7。
该试验对结直肠癌患者产生的主要结果是
-
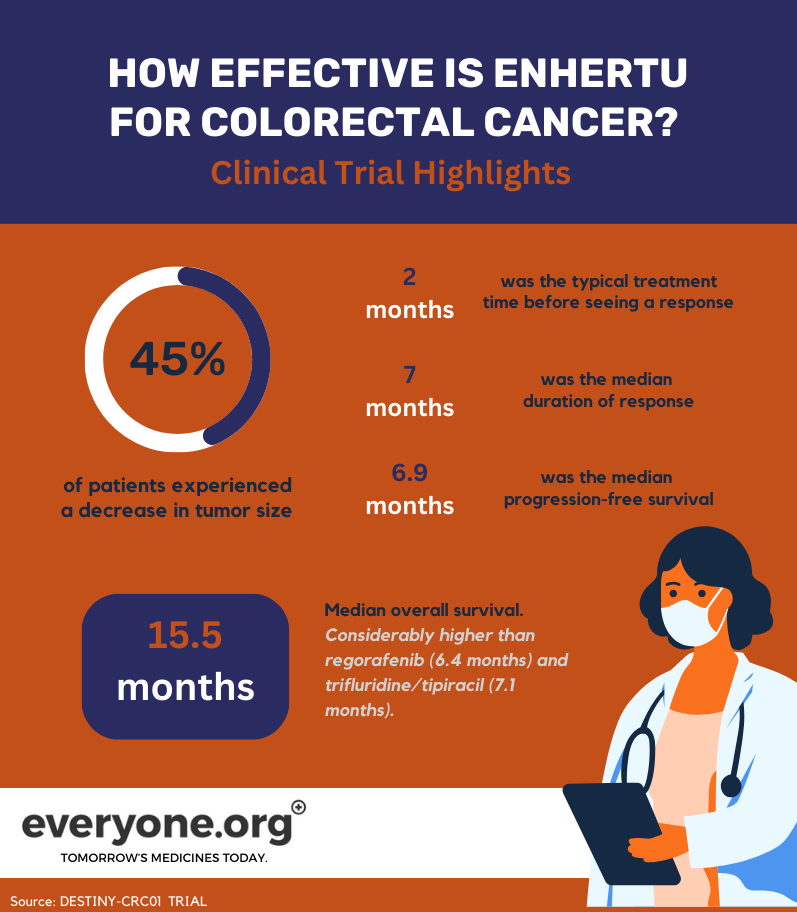
在接受Enhertu 治疗的患者中,45.3% 的肿瘤部分缩小;
-
治疗反应一般在治疗开始后 2 个月左右出现;
-
中位应答持续时间为 7 个月;
-
无进展生存期的中位数为 6.9 个月;
-
中位总生存期为 15.5 个月。这一结果大大超过了目前的治疗标准。例如,regorafenib 和trifluridine/tipiracil 是常见的三线疗法。这些疗法的总生存期分别为 6.4 个月和 7.1 个月。
另一项名为 DESTINY-CTC02 的试验正在研究Enhertu 对结直肠癌患者的治疗效果。该试验仍在进行中,但其初步结果与 DESTINY-CTC01 试验的结果一致10。

Enhertu 治疗大肠癌的安全性如何?
在安全性方面,这些是 DESTINY-CRC01 试验的主要结果:
-
每位患者都有治疗的副作用。最常见的副作用是胃病和血液问题。
-
37.7% 的患者出现了严重的不良反应。最常见的严重副作用是中性粒细胞计数低(22.1%)和贫血(14%)。
-
7%的患者在停药后会出现间质性肺病(ILD)这种副作用。
-
报告了 3 例与药物相关的死亡病例,均与间质性肺病有关。
这意味着什么?
Enhertu不同患者组之间的安全性结果无法直接比较。不过,为了帮助您了解具体情况,以下是Enhertu 在多种肿瘤类型中的安全性结果摘要。包括Enhertu 已获批治疗的肿瘤:
-
12%的试验患者出现了 ILD,1.5%的病例出现了致命后果;
-
34.6%的试验患者出现中性粒细胞计数下降;
-
34-43% 的试验患者出现贫血(取决于药物剂量)8.
有鉴于此,Enhertu 治疗结直肠癌的安全性与其治疗其他获批癌症的安全性相似。
Enhertu 何时获批用于治疗结直肠癌?
Enhertu 用于 HER2 阳性结直肠癌的批准没有明确的时间表。
DESTINY-CRC02 试验正在进行中,最终结果预计将于 2024年 7 月公布。如果结果乐观,FDA 可能很快就会批准Enhertu 用于治疗结直肠癌。它的突破性认证有助于加快这一进程。
但结直肠癌患者不必等到 2024 年末才能访问Enhertu 。与此同时,Enhertu 在您的 CRC 治疗中能发挥什么作用?
医生能给我开Enhertu 治疗结肠直肠癌吗?
目前最好的答案是:也许吧。
Enhertu 在任何地方都未被批准用于 HER2 阳性结直肠癌的治疗。不过,无论如何,您的医生都有权为这一适应症开药。他们可以根据 DESTINY-CRC01 试验的最终结果或 DESTINY-CRC02 试验的初步结果以及您的具体情况来开药。
如果医生给你开的药没有被批准用于治疗某种疾病,这就是标示外使用。在某些国家,由于当地法规和供应情况的限制,开具标示外使用处方可能具有挑战性。不过,使用 "指定患者进口条例 "配药总是可行的。
您的医生是否已决定为您开Enhertu 治疗结肠直肠癌?我们在 www.everyone.org 的团队可以帮助您获得药物。我们专门从事采购和交付未经批准或患者所在国无法获得的处方药。请联系我们,以便我们为您提供帮助。
参考文献:
- Barrie, Robert.Enhertu 赢得两项 FDA 突破性疗法认定。制药技术》,2023 年 8 月 31 日。
- FDA 授予曲妥珠单抗德鲁司坦治疗 HER2+ 实体瘤(包括 mCRC)的突破性疗法认定。OncLive,2023 年 8 月 31 日。
- 突破性疗法。美国食品和药物管理局,2018 年 1 月 4 日。
- Enhertu | 欧洲药品管理局。欧洲药品管理局,2023 年 10 月 30 日访问。
- Stewart, Judith.Enhertu (fam-trastuzumab deruxtecan-nxki)FDA 批准历史。 Drugs.com,2022 年 8 月 15 日。
- 结肠癌中的 HER2 生物标志物。了解您的生物标志物》,2023 年 5 月 24 日。
- DESTINY-CRC01研究曲妥珠单抗德鲁司坦治疗HER2表达转移性结直肠癌患者的最终结果。自然通讯》,2023 年 10 月 30 日访问。
- Enhertu, INN-trastuzumab deruxtecan.欧洲药品管理局 , 2023 年 10 月 30 日访问。
- 曲妥珠单抗地屈孕酮治疗 HER2 表达晚期或转移性结直肠癌患者(DESTINY-CRC02)。ClinicalTrials.gov,2023 年 10 月 30 日访问。
- 曲妥珠单抗德鲁司康(T-DXd)治疗HER2-表达异常/扩增(HER2+)转移性结直肠癌(mCRC)患者(pts):多中心、随机、2 期 DESTINY-CRC02 研究的初步结果。临床肿瘤学杂志》,2023 年 10 月 30 日访问。