英国有dostarlimab 吗(同时该怎么办)?
最后更新2024 年 2 月 05 日

你可以合法地获得新药,即使它们在你的国家没有得到批准。
了解更多 "Dostarlimab (Jemperli )是一种新型抗 PD-1 疗法。它于 2021 年获得了欧洲医学管理局(EMA)和英国皇家药品管理局(MHRA)的有条件上市许可,用于治疗晚期或复发性子宫内膜癌[1, 6]。由此,它成为欧洲首个获批用于该适应症的抗PD-1疗法。
对于错配修复缺陷(dMMR)肿瘤患者来说,这是一个重要的里程碑。葛兰素史克公司英国肿瘤副总裁杰克-哈里斯(Jack Harris)表示[2],尤其是因为该领域的创新一直滞后。
不过,那些急于在英国开始dostarlimab 治疗的人可能需要多一点耐心。这种药物还需要一段时间才能在市场上广泛销售。
dostarlimab 在英国获得批准了吗?
目前,dostarlimab 已获批准,但尚未在英国市场上广泛销售。
Dostarlimab 在英国只能通过 "药品早期使用计划"(EAMS)获得 [4]。通过 EAMS 获得药品并不等同于获得 MHRA 的正式批准。该计划旨在为没有有效治疗方案的严重疾病或病症提供早期新药。
值得注意的是,dostarlimab 只能通过 EAMS 用于治疗 dMMR/MSI-H 原发性晚期或复发性子宫内膜癌。其另一个经 FDA 批准的适应症,即治疗 dMMR/MSI-H 晚期或复发性实体瘤,在英国尚未得到认可。
dostarlimab 是否在国家医疗服务系统中提供?
2022 年 2 月,英国国家医疗服务系统(NHS)宣布,每年将为约 124 名患有 dMMR/MSI-H 型子宫内膜癌的妇女提供dostarlimab 。
美国国家健康与护理优化研究所(NICE)支持dostarlimab 用于曾接受过铂类化疗的患者。
Dostarlimab列入癌症药物基金后,可以收集更广泛的数据和长期证据。不过,目前dostarlimab 尚未被推荐用于国家医疗服务体系的常规治疗。
如果您不是每年提前获得这种新型免疫疗法的 124 名妇女之一呢?或者,如果您需要药物治疗 dMMR/MSI-H 实体瘤而不是子宫内膜癌呢?在这种情况下,英国国家医疗服务系统(NHS)目前无法为您提供dostarlimab 。
dostarlimab 何时在英国上市?
获得 MHRA 的有条件上市许可只是dostarlimab 进入英国市场的第一步。还需要考虑和决定当地的定价以及国民保健服务的全面覆盖范围[5]。
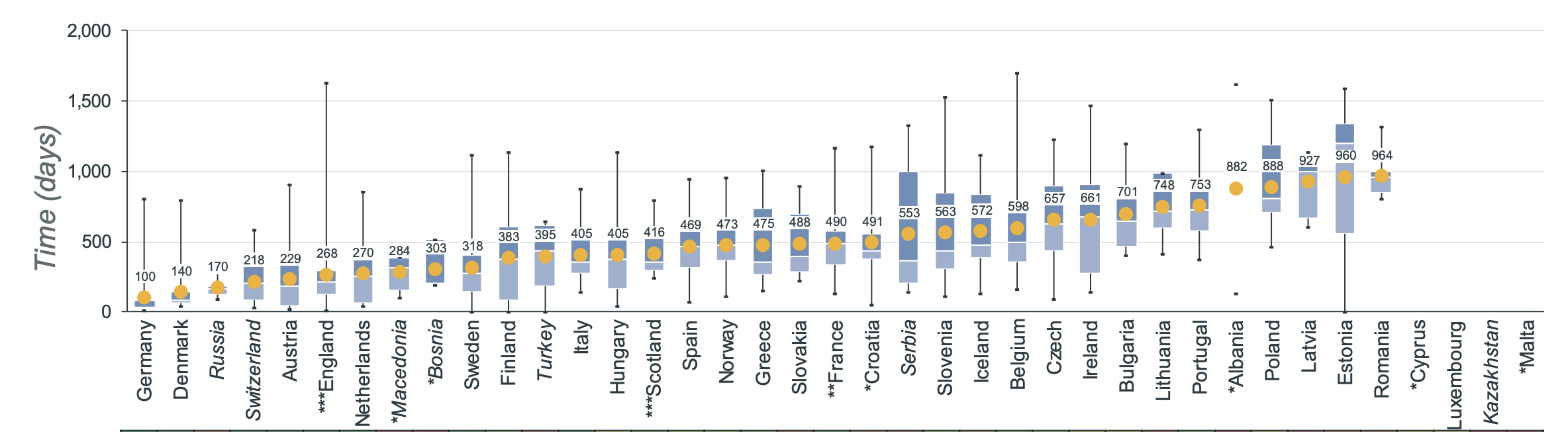
一种药物从获得 EMA 批准到上市所需的平均时间,在不同国家有很大差异。2022 年,欧洲肿瘤治疗药物从获得 EMA 上市许可到广泛上市的平均时间为 511 天。英国的平均上市时间为 268 天,爱尔兰为 661 天[3]。
在这种情况下,dostarlimab 可能还需要一段时间才能在英国市场上普及。

如何在英国获得dostarlimab ?
您是英国的子宫内膜癌或晚期 dMMR/MSI-H 实体瘤患者吗?如果您的医生建议您使用dostarlimab 进行治疗,但您不符合提前获得治疗的条件,您仍有其他选择。
如果某种药品在患者所在国未获批准,或已获批准但尚未上市(如dostarlimab 在英国的情况),您可以通过 "指定患者进口 "条例获得该药品。
Everyone.org 专门帮助人们通过该条例获取最新药物。如果您有主治医生开具的Jemperli (dostarlimab)处方,您急于开始治疗计划,并希望我们帮助您立即获得药品,请联系我们。
参考文献:
- Jemperli | 欧洲药品管理局。欧洲药品管理局,2021 年 4 月 21 日。
- Cooper, Emma.英国患者获准提前接受葛兰素史克的子宫内膜癌治疗。Pf Media,2023 年 7 月 10 日。
- EFPIA 2021 年患者 W.A.I.T. 指标调查。EFPIA,2023 年 9 月 25 日访问。
- 早期获取药品的科学意见--公共评估报告 产品Dostarlimab EAMS适应症Dostarlimab 。英国政府,2023 年 6 月 29 日。
- Ewbank, Leo.英国国家医疗服务体系中新药的获取。国王基金,2020 年 10 月 28 日。
- Parsons, Lucy.葛兰素史克的 PD-1 抑制剂Jemperli 在英国获批。医药时报》,2021 年 6 月 7 日。